SOMATOM Drive : Drive Precision for all
最新型Dual Source CT「SOMATOM Drive」の臨床活用について
吉田守克(一般社団法人天草郡市医師会立 天草地域医療センター放射線科)
<Session Ⅴ Focus on New Performance of Dual Source CT>
2017-11-24

当センターは,熊本県西端に位置する天草地域の高度医療を支える中心的役割を担っている。一般臨床のみならず,救急医療全般に対応しうる体制が求められており,高性能で汎用性の高い高度医療機器の整備が図られている。
当センターは病床数210床,年間検査件数はCTが8000件,MRIが3000件ほどである。CT検査は2台体制で行っており,うち1台を2017年2月にシーメンスのDual Source CT「SOMATOM Drive」に更新した。最上位機種「SOMATOM Force」の技術を継承したSOMATOM Driveは,検出器「StellarInfinity Detector」と新型X線管「STRATON MX Sigma」を搭載し,低被ばくで高精細なCT検査が可能となっている。
本講演では,SOMATOM Driveを選定したポイントや導入による臨床上の変化,実際の使用状況について報告する。
SOMATOM Drive選定に際して考慮したポイント
CT装置の更新にあたっては,高速撮影,時間分解能,被ばく低減,金属アーチファクト低減,Dual Energy CT(DECT)をポイントに検討し,SOMATOM Driveを選定した。
●高速撮影
高速撮影においては,検出器幅の2倍を超える速度は出せないSingle Source CTと比べ,Dual Source CTであるSOMATOM Driveの“Drive Spiral Scan”では検出器幅の3倍以上の速度を出すことができ,臨床上のメリットは大きい。
症例1(図1)は大動脈弓部の動脈瘤で,Single Source CTの画像(a)と比較すると,SOMATOM Driveの画像(b)では上行大動脈の動きが抑制され,クリアな画像を得られていることがわかる。特に,救急で大動脈解離が疑われるような症例で有用である。
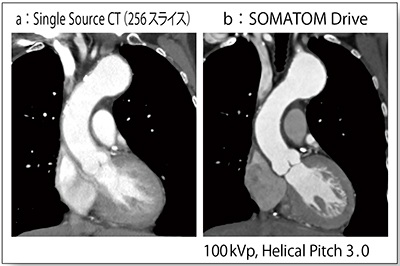
図1 症例1:大動脈弓部の動脈瘤(78歳,女性)
●時間分解能
SOMATOM Driveの75msという高い時間分解能は,心臓撮影において非常に威力を発揮する。症例2は,虚血性心疾患疑いの症例であるが,心拍数が100bpmほどであっても,拍動の影響が非常に少ない画像を得ることができている(図2)。
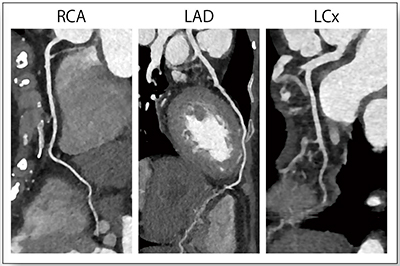
図2 症例2:虚血性心疾患疑い(56歳,女性,HR:100bpm)
●被ばく低減
被ばく低減技術としては,低電圧撮影およびTin filterが使用可能である。
低電圧撮影と逐次近似画像再構成法の組み合わせは,被ばく低減,造影剤使用量低減に有用であることが知られている。当センターでは以前から,80kVの低電圧撮影を使用して被ばく低減および造影剤使用量低減に努めてきたが,SOMATOM Driveではさらに低い70kV撮影も使用できるようになり,さらなる被ばく低減,造影剤使用量低減が可能になった。STRATON MX Sigmaにより2管球合わせて最大1600mAの出力が可能で,70kV撮影でも臨床に耐えうる画像が得られる。また,Tin filterを使った“Spectrum Shaping技術”では,低エネルギー成分を除去することで被ばくやノイズを低減できるとともに,ピークが高エネルギー側にシフトすることでビームハードニングアーチファクトの抑制も可能である。
症例3(図3)は肝細胞がん治療後の症例である。腎機能障害のため70kV,240mgI/kgにて撮影を行った。外側区域に単純CT(図3 a)で低吸収,造影CT(図3 b,c)ではearly enhancementを示す腫瘍が認められ,再発が疑われた。70kV撮影,240mgl/kgの造影剤量でも,腫瘍,大動脈,門脈の造影効果は十分に得られ,被ばく線量も通常の120kV撮影と比べ40%ほどに抑えられている。
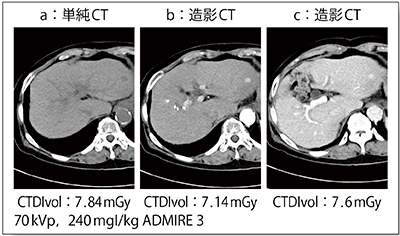
図3 症例3:肝細胞がん再発疑い(75歳,女性)
症例4は,原発性肺がん疑いで当センターにて肺生検を施行し,翌日にTin filterプロトコルで気胸のフォローアップ撮影を行った。胸部単純X線を数枚撮影した程度の線量で明瞭な画像を得られている(図4)。現在当センターでは,肺生検後のフォローアップはすべてSOMATOM DriveのTin filterプロトコルで実施している。
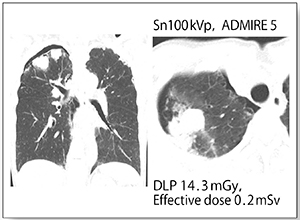
図4 症例4:原発性肺がん疑いで肺生検施行後
(60歳,女性)
●金属アーチファクト低減
SOMATOM Driveでは“iMAR”(金属アーチファクト低減ソフトウェア)を使用できることに加え,Tin filterやDECTと組み合わせることで,金属アーチファクトをより低減することができる。iMARでは,ターゲットとするデバイス(コイルやインプラントなど)を選択して適用することで,最適なアーチファクト低減効果を得ることができる。
症例5は左人工骨頭ステム周囲骨折術後で,仮骨の状況などを詳細に観察するためCTを撮影した。iMARによりアーチファクトが抑制され,非常にクリアで評価しやすい画像を得ることができた(図5)。
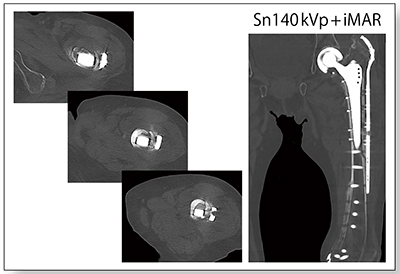
図5 症例5:左人工骨頭ステム周囲骨折術後(77歳,女性)
●Dual Energy CT(DECT)
当センターでは,悪性腫瘍や外傷,イレウス症例などにDECTを活用している。
症例6(図6)の膵がん疑い症例では,mixed image(従来の読影画像:a)と比べ,仮想単色X線画像“DE Monoenergetic Plus(Mono+)”による50keV画像(b)では,膵がんの描出能が非常に上がっていることがわかる。
このほか,“DE Bone Marrow” imageによる骨折の新旧の鑑別(図7),Iodine mapによる絞扼性イレウスの診断(図8)など,DECTの臨床的有用性は非常に高い。
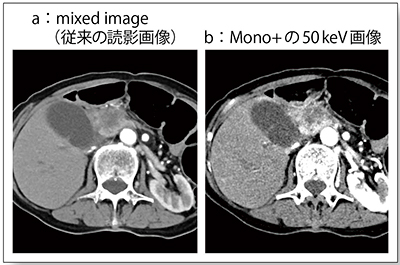
図6 症例6:膵がん疑い(80歳,女性)
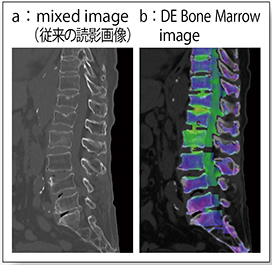
図7 腰椎圧迫骨折(74歳,女性)
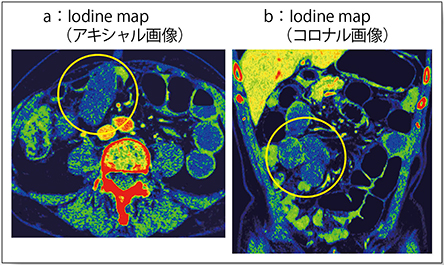
図8 絞扼性イレウス(80歳,男性)
SOMATOM Drive導入による変化
SOMATOM Driveでは,Drive Spiralによる息止め不良への対応,DECTによる機能的診断,70kV撮影やTin filterによる被ばく低減や造影剤量低減,Tin filterやDECTとiMARを併用した金属アーチファクト除去などを実現し,より高画質・低侵襲で,臨床的に有用な検査が可能になった。撮影条件の選択肢が増えたことで,患者にとってより良い検査を追究できるようになり,研究や発表に対する医師や診療放射線技師のモチベーションが非常に向上した。
また,息止め不可や心拍数が高い患者など,以前であれば診断可能な画像の取得が難しかった症例でも,良好な画像を得られるようになった。SOMATOM Driveが稼働した2017年2月以降の半年間で,読影所見でpoor imageとされた件数は2台で12件(SOMATOM Drive導入前の前年同期間では36件)あったが,うちSOMATOM Driveは1件のみであった。SOMATOM Driveの1件は,認知症がある高心拍の患者の冠動脈CTという条件の厳しい検査であり,SOMATOM Driveではほぼすべての検査でクリアな画像が得られると言っていいだろう。
臨床上の変化としては,検査フローの変化が挙げられる。例えば,新旧椎体圧迫骨折の診断において,形態画像のみでは評価困難な椎体圧迫骨折ではMRI検査が施行されるが,SOMATOM DriveによるDECTのDE Bone Marrow imageを導入してからは,DECTが第一選択となり,評価できない場合にのみMRI検査を施行する流れとなった。
当センターでのSOMATOM Driveの使用状況
SOMATOM Drive導入後半年間の検査数は4559件で,前年同時期(4372件)とあまり変わらないが,導入後は全検査の75%をSOMATOM Driveで施行している。これは,SOMATOM Driveでは症例を選ばずに高画質が得られること,低被ばく・高画質が両立すること,DECTによる機能的評価ができることの3つが大きな要因であると考える。
SOMATOM Driveで撮影を行った3405件のうち,肺野などの限定された領域を除き,90%近くでDual Source mode(Dual Energy,Dual Power,Drive Spiralなど)を施行している。Dual Source CTはスループットが低下するのではないかと懸念する声もあるが,当センターの経験ではそのようなことはなく,どのような状況でもDual Source modeを使えることがSOMATOM Driveの利点である。
まとめ
SOMATOM Driveは,SOMATOM Forceなど上位機種の技術を投入して開発された最新型Dual Source CTである。日常検査でもスループットを落とさずにDual Source modeを使用することができ,症例を選ばずに良好な画像を得ることができる。加えて,研究や発表に対する医師や技師のモチベーション向上というメリットももたらしている。
- 【関連コンテンツ】
